Sebadenitis - eine mysteriöse HautkrankheitPD Dr. Ina Pfeiffer Aktueller Überblick Aktueller Überblick
Bei der Sebadenitis (SA) des Hundes handelt es sich primär um eine fortschreitende entzündliche Zerstörung der Hauttalgdrüsen. Es wurde beobachtet, dass die Krankheit bei verschiedenen Rassen sowie auch bei Mischlingen vorkommt. Dabei fällt eine gewisse Prädisposition auf.
Anatomie der Haut - die Talgdrüse
Wie bereits erwähnt, spielen die Talgdrüsen der Haut (Glandulae sebaceae) eine zentrale Rolle bei dieser Gesundheitsproblematik.
Klinische Anzeichen
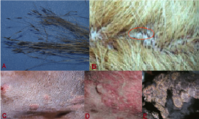
Die idiopathische (= ohne erkennbare Ursache) Sebadenitis wird charakterisiert durch die Entzündung der Talgdrüsen. Mikroskopische Untersuchungen zeigen bei SA ein trockenes und schuppiges Hautbild. Charakteristisch für die Sebadenitis beim Akita sind ferner die eng am Haarschaft anhaftenden, oftmals bräunlich verfärbten und verklebenden Schuppen („Manschetten“) (Abb. 3). Neben einem Verlust der Unterwolle wird das Fell als trocken, glanzlos und brüchig (Box 1) beschrieben (Sousa, 2006). Das Ausbleiben des Sebums verursacht in der Regel eine Reihe von Sekundärinfektionen der Haut, z.B. mit Bakterien, Viren oder Pilzen (Bensignor und Guaguère, 2012). Damit verändert sich der Eigengeruch der Hunde: Sie riechen wie „drei Tage getragene Socken“. Die ersten Krankheitsanzeichen treten in der Regel am Kopf, an der Ohrmuschel (braune krümelige Ablagerung, verwechselbar mit Milben) und am Rücken auf. Die Symptome breiten sich später über den kompletten Körper bis zum Schwanz aus (Simpson und McKay, 2012). In der chronischen Erkrankungsphase erscheint das Fell dünner, „Mottenfraß‑ähnlich“ (Simpson und McKay, 2012), die übrig gebliebenen Haare schimmern grau und ähneln beinahe einem „Welpenflaum“.
Abb. 4: A-E: Darstellung des Krankheitsbildes von Sebadenitis bei Akita:
A: "Federartige" Keratinmanschetten (Bensignor u. Guaguère, 2012) B: Keratinmanschetten am Haaransatz (roter Kreis) C: Blasen (Papeln) (Noli,2008), D: Pusteln (Noli, 2008) E: Schuppenkränze (Noli, 2008) Beim Akita tritt dazu gelegentlich eine diffuse Hyperkeratose (griech: Hyper „Über“, keratos „Horn“) und eine symmetrische Alopezie (Haarausfall) auf (Bensignor und Guaguère, 2012). Demnach ist es nicht gelungen den Krankheitsgrad am Alter des Hundes auszumachen. Beim Akita geht man davon aus, dass es sich bei SA wahrscheinlich um ein autosomal-rezessives Vererbungsmuster (Abb. 5) handelt (Reichler, et al., 2001). Von daher wird öfters der Begriff einer Genodermatose (Geno = genetisch bedingt, dermatose = Hauterkrankung) diskutiert. Als Auslöser der Sebadenitis spielt vermutlich ein Hormonwechsel eine Rolle. DiagnostikEine zweifelsfreie Diagnose, ohne Hautbiopsie, fällt bei SA oft schwer. Es bestehen zahlreiche Ähnlichkeiten zu anderen Krankheitsbildern wie z.B.: Canine Demodikose (parasitäre Hauterkrankung), Dermatophytose (Hautpilzerkrankung), Follikulitis (Follikelentzündung) oder Leishmaniose (Infektionskrankheit) (Bensignor und Guaguère, 2012).
BiopsieBei Verdacht auf eine Sebadenitis werden, um sich größtmögliche Gewissheit zu verschaffen, mehreren Hautbiopsien präpariert. Dabei entnimmt man Gewebeproben aus verschiedenen Körperarealen, um die Entzündungsphasen der Talgdrüsen zu identifizieren. Bei diesen Zellen handelt es sich um Makrophagen, Lymphozyten, Plasmazellen und neutrophile Granulozyten. Fachsprachlich wird dieser Zustand als perifollikuläres (= um den Follikel herum) Granulosom bezeichnet und steht für eine Ansammlung von vielen Zellen ohne Bindegewebe (Linek, et al., 2005). TrichoskopieIn der Trichoskopie (griech. Trichos „Haar“, alt.griech. skopein „skopie“ = Gerätetechnik), werden die Haare untersucht. Bei der Analyse wird dem Hund Fell entnommen und unter dem Mikroskop beurteilt. Dabei verschafft man sich einen Überblick zur Haardichte, Schuppen- oder Pustelbildung und über die SA für charakteristischen Keratinmanschetten (Bensignor und Guaguère, 2012).
BehandlungBisher gibt es keine kurative Behandlung, die mit 100%iger Sicherheit gegen Sebadenitis hilft (Bensignor und Guaguère, 2012). Anders ausgedrückt, gibt es keinen bekannten Behandlungsweg, der den betroffenen Akita vollständig heilen kann. Lokale BehandlungenUnter einer lokalen Behandlung versteht man die äußere Anwendung von Medikamente. Im folgenden werden die einzelnen Therapie‑Stufen erläutert. Sie ist mit 4 Stufen relativ zeitaufwändig, jedoch außerordentlich erfolgsversprechend, wie sich in der Praxis gezeigt hat (Simpson und McKay, 2012). 1. Stufe: Ziel: Hautschuppen, die Krusten und Keratinmanschetten abzulösen. Der Hund sollte mit einem keratolytischen oder keratoplatischen Shampoo gebadet werden. Es handelt sich hierbei um Vorgänge, die den Abbau von trockenen Schuppen und Krusten ermöglichen und den Wiederaufbau gesunder Hautschuppen fördern. Dabei sind Waschlotionen, mit z.B. Schwefel oder Salicylsäure (Scott, et al., 2001), als Wirkstoff empfehlenswert. Im Falle einer sekundär entstandenen Follikulitis können Kombinationsprodukte, auf Basis von Dibenzoylperoxid, hinzugenommen werden. Sämtliche Mittel sollten ca. 10 Minuten auf die Haut einwirken, bevor diese wieder abgespült werden (Simpson und McKay, 2012). 2. Stufe: Ziel: Wiederaufbau der Lipidbarriere der Hornschicht (Stratum corneum) Nach einer Behandlungszeit von ca. zwei Stunden, wird in Stufe 3 das überschüssige Öl abgebraust. 4. Stufe: Ziel: Hautpflege Ein Erfolg der Prozedur kann jedoch nicht garantiert werden. Bei der Mehrzahl der Hunde schlägt die Behandlung gut an und es kommt zum erneuten Haarwuchs und einer gewissen Gesundheitsstabilisierung. Bei anderen Individuen jedoch zeigt sich keine deutliche Verbesserung. Wie Analysen gezeigt haben, ähneln die Bestandteile des Olivenöls (bis 83% Ölsäure) der natürlichen Zusammensetzung des Sebum: 48% Cholesterinester, 48% Wachse, Diester und 4% Fettsäuren sowie ein leicht saurer pH‑Wert (Bensignor und Guaguère, 2012). Somit kann Olivenöl anstelle des Sebums den äußeren Biofilm der Haut simulieren und gegen schädliche Erreger schützen (Bensignor und Guaguère, 2012). Zu den kostspieligen Medikamenten gegen SA gehören, die mit Nebenwirkung behafteten, Cyclosporine. Sie zählen zur Gruppe der Immunsuppressiva. Diese Mittel werden zur Unterdrückung des Immunsystems eingesetzt. Bislang war lediglich die orale Einahme von Cyclosporin geläufig. Nach einer aktuellen Studie, können Cyclosporine auch als Spray verwendet werden. Dabei konnte ebenfalls eine Verbesserung des Allgemeinenzustandes des Hundes beobachtet werden. Ferner wird ein Arzneimittel zur Behandlung von Hundeohren, namens Ortena® (Hauptbestandteil 1,2‑Propandiol), als wirksames Medikation diskutiert. Systemische BehandlungUnter systemischer Behandlung versteht man das Verabreichen von Medikamenten als Tablette oder Injektion, so dass der Wirkstoff über den Blutkreislauf in den gesamten Körper zum Wirkungsort gelangen kann. Kritische BehandlungenEinige systemische Behandlungsmethoden zeigen unbefriedigende Therapieergebnisse bezüglich SA. Ebenfalls enttäuschende Resultate werden mittels der Corticoid-Behandlung erzielt (Bensignor und Guaguère, 2012; Simpson und McKay, 2012). Als letzte Therapie gibt es noch die Behandlung von SA mit Vitamin A (Retinoid). Wie die vorherigen Medikamente, weist Vitamin A ebenso einen entzündungsreduzierenden Effekt auf. Zudem sind Retinoide bei der Vermehrung und Differenzierung von Zellen beteiligt. Behandlung einer sekundär verursachten Mikrobiellen‑InfektionDie durch SA entstandenen Hautläsionen (Hautverletzung) der Akita können sich oftmals zusätzlich durch den Befall von Bakterien, Viren oder Pilze entzünden. ForschungsperspektivenAufgrund der ungeklärten Krankheitsursache von SA beim Akita, eröffnet sich generell ein breites Forschungsfeld. Von enormer Wichtigkeit und, um den Anschluss nicht zu verlieren, ist für unsere Arbeit die Unterstützung von Züchtern und Haltern unumgänglich: Es bleibt eine offene Frage, aus welchem Gründen bei SA die Abwehrzellen des Hundes körpereigene Strukturen angreifen und vernichten. Eine Dauergabe von Immunsuppressiva (z.B. Cyclosporin), ist erst mal bezüglich der hohen Kosten und unerwünschten Nebenwirkungen keine langfristige Lösung. Fragen, die es zu klären gilt, sind z.B. welche Verbindungen rufen die Auto-Immunreaktionen an den Talgdrüsen hervor? Ebenfalls muss herausgefunden werden, welche genetischen Ursachen für die Fehlregulation der Prozesse verantwortlich sind. Da das Immunsystem sehr komplex ist, müssen hierbei verschiedenste Motive und Möglichkeiten in Betracht gezogen werden. Da es sich bei SA um eine ausgesprochen vielschichtige Problematik handelt, ist sicher auf genetischer Ebene von keiner einfachen und kurzfristigen Lösung auszugehen.
Bensignor, E. und Guaguère, E. (2012). Adénite sébacée granulomateuse du chien : une revue. Brüggemann, A. (2014). Tibet Terrier. Abgerufen am 5. März 2014 von http://www.tibet‑terrier‑wissen.de/gesundheit/erbkrankheiten Fabre, P. (2014). Akne muss kein Schicksal sein. Abgerufen am 15. Februar 2014 von http://www.akne‑info.ch/alles‑ueber‑akne/akne‑verstehen/ Käser, H. (2014). olionatura. Abgerufen am 4. März 2014 von http://www.olionatura.de/_oele/index.php?id=33 Klöppel, G., Rudolph, P., Mentzel, T., Cardesa, A., Kreipe, H. H., Slootweg P. J., Remmele, W. Linek, M., Boss, C., Haemmerling, R., Hewicker‑Trautwein, M., & Mecklenburg, L. (2005). Noli, C. (2008). Papeln, Pusteln, Krusten beim Hund‑Algorithmus. Ospedale Veterinario Cunesse. Italien. Reichler, I. M., Hauser, B., Schiller, I., Dunstan, R. W., Credille, K. M., Binder, H., Claus T.,Arnold S. (2001). Sebaceous adenitis in the Akita:clinical observations, histopathology and heredity. Veterinary Dermatology (12), S. 243‑253. Rosser, E. J. (1999). Therapy for sebacous adenitis. In: Bonagura JD, ed. Kirk‘s Current Scott, D. W., Miller, J. und Griffin, C. E. (2001). Dermatologic therapy. In: Muller and Kirk‘s Simpson, A. und McKay, L. (2012). Sebaceous Adenitis in Dogs. Vetlearn , E1‑E7. Sousa, C. A. (2006). Sebaceous adenitis. Vet Clin North Am Small Anim Pract (36), S. 243‑9
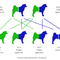
autosomal rezessives Vererbungsmuster: Beim autosomal-rezessiven Erbgang werden Defektgene, die für die Ausprägung des gleichen Merkmales verantwortlich sind von den Elterntieren an die Nachkommen weitergegeben. Nur wenn beide Elterntiere das Defektgen weitergeben, kommt die Erkrankung zum Ausbruch. Erbt eine Nachzucht nur ein verändertes Gen vom Rüden oder von der Hündin, erkrankt sie nicht selbst, vererbt dieses Gen aber an die eigenen Nachkommen weiter. Meist sind beide Elternteile "gesund" und heterozygot und geben das kranke Gen an die Nachkommen weiter. Ein Nachkomme kann bei einem autosomal-rezessiven Erbgang, nur erkranken, wenn beide Elterntiere (Rüde und Hündin) Träger des defekten Allels sind. So kann die Krankheit auch mal mehrere Generationen überspringen, bevor sie wieder zum Ausbruch kommt. Die Wahrscheinlichkeit, von der Erbkrankheit betroffen zu sein, liegt für die Nachkommen bei 25 %. Ist ein Elterntier bereits erkrankt, bzw. die Krankheit zum Zeitpunkt der Verpaarung noch nicht ausgebrochen, so steigt die Wahrscheinlichkeit der Nachkommen ebenfalls zu erkranken auf 50 % an. Sind beide Elterntiere von der Erbkrankheit betroffen, ohne dass diese zum Zeitpunkt der Verpaarung bereits ausgebrochen ist, werden 100% der Nachkommen ebenfalls unter der Erbkrankheit leiden, unabhängig vom Geschlecht. |